Maladie de Castleman et diagnostic différentiel
Publié le 9 avr. 2021 • Par Charlotte Avril
La maladie de Castleman est une pathologie non maligne rare. Elle est définie par une image du tissu ganglionnaire particulière associée à des éléments cliniques et biologiques.
Il en existe plusieurs formes distinctes, tant dans la présentation que dans leur prise en charge. Pour en savoir plus, rendez-vous sur notre article “Maladie de Castleman : tout ce que vous devez savoir”. Certaines pathologies (hémopathies, maladies auto-immunes, infections) peuvent s’accompagner de lésions ressemblant à celles observées dans la maladie de Castleman.
Quelles sont les pathologies considérées comme des diagnostics différentiels de la maladie de Castleman ?

Tout d’abord, qu’est ce qu’un diagnostic différentiel ?
C’est une méthode permettant de différencier une maladie d'autres pathologies qui présentent des symptômes ou caractéristiques proches ou similaires. Ce procédé a pour objectif d’établir un diagnostic plus sûr par une approche méthodique consistant à tenir compte tant des éléments permettant d'exclure une maladie plutôt que ceux permettant de la confirmer.
Comment diagnostiquer une Maladie de Castleman ?
Le diagnostic va essentiellement reposer sur un examen anatomo-pathologique effectué à partir d’une biopsie, la plupart du temps ganglionnaire. Cet examen consiste en une analyse macroscopique et microscopique du tissu, qui va étudier le type de cellules, son caractère cancéreux ou non cancéreux ainsi que son agressivité (le grade).
Dans la maladie de Castleman (MC), les lésions associent, à des degrés variés selon les formes anatomo-pathologiques :
- Une hyperplasie folliculaire : consistant en un volume anormalement important des follicules (agrégats de lymphocytes ou globules blancs) dans les ganglions.
- Une régression des centres germinatifs : les centres germinatifs étant les zones ganglionnaires dans lesquelles les lymphocytes B activés (globules blancs responsables de la production des anticorps) prolifèrent.
- Une expansion ou désorganisation du réseau des cellules folliculaires dendritiques : les cellules dendritiques sont impliquées dans le déclenchement des réponses immunitaires. Sentinelles de l’organisme, elles servent à détecter des agents pathogènes tels que des bactéries et des virus et à l’activation des lymphocytes T (qui détruisent les cellules infectées).
- Des capillaires hyalinisés : la hyalinisation est la destruction du collagène dans les capillaires (petits vaisseaux sanguins), leur donnant un aspect transparent comme du verre.
- Expansion de la zone du manteau : dans le ganglion lymphatique, le manteau est la zone entourant le centre germinatif.
- Hyperplasie vasculaire interfolliculaire : volume anormalement important des vaisseaux dans l’espace entourant les follicules.
- Hyperplasie plasmocytaire interfolliculaire : volume anormalement important de plasmocytes (cellules dérivées des lymphocytes sécrétant activement des anticorps) dans l’espace entourant les follicules.
- Fibrose périvasculaire ou périphérique : la fibrose est la modification anormale des tissus de notre organisme.
Dans le Protocole National de Diagnostic et de Soins (PNDS) concernant la maladie de Castleman (MC) de la Haute Autorité de Santé (HAS) (2019), on retrouve des descriptions imagées de certains de ces aspects anatomo-pathologiques. Toutefois la HAS précise qu’ils ne sont pas spécifiques de la lésion de Castleman.
- L’aspect en «Bulbe d’oignon» ou «Onion-skin» fait référence à l’hyperplasie de la zone du manteau folliculaire
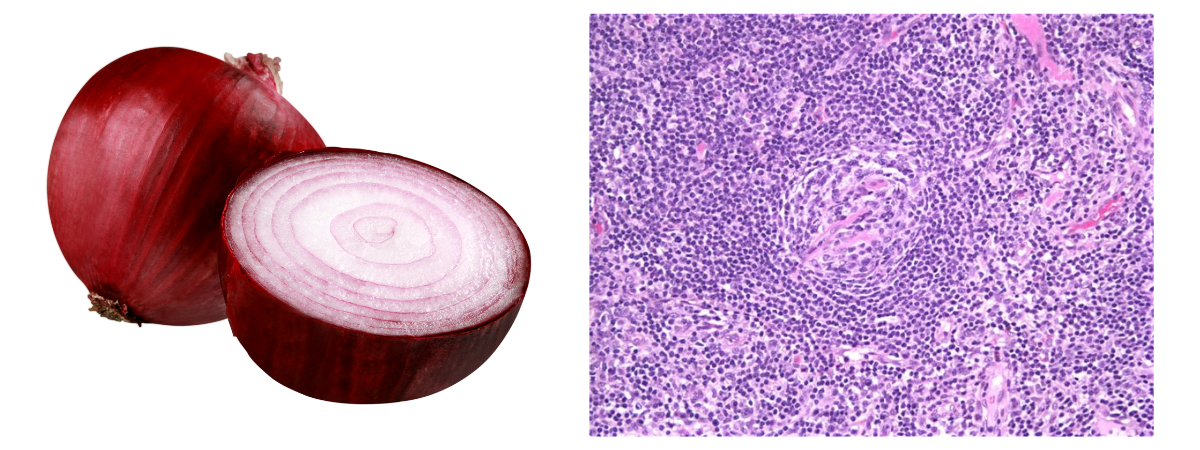
- L’aspect en «Sucette» ou «Lollipop» fait référence aux centres germinatifs pénétrés par des vaisseaux hyperplasiques
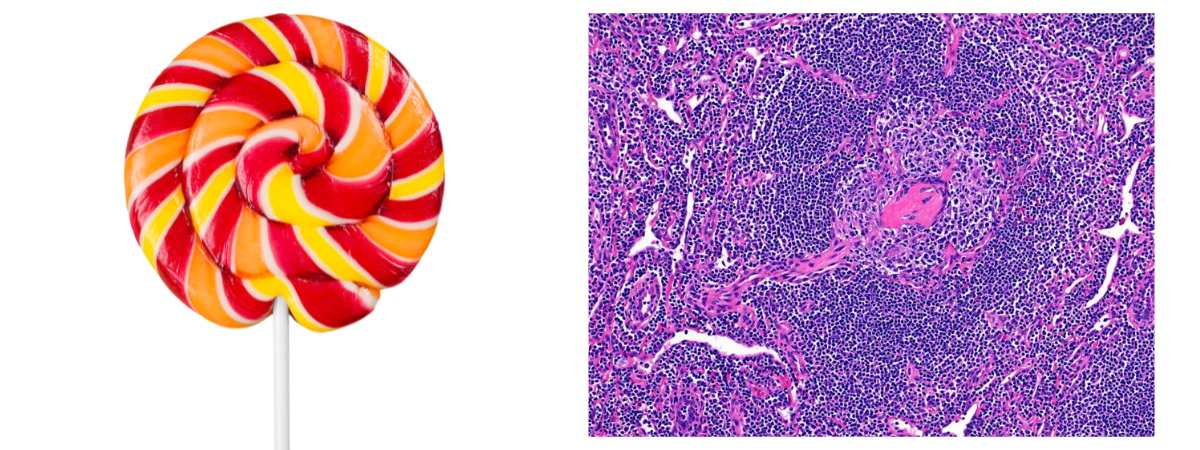
- L’aspect en «Menottes» ou «Budding», «Twinning», «Handcuff» fait référence à des follicules pouvant contenir deux centres germinatifs
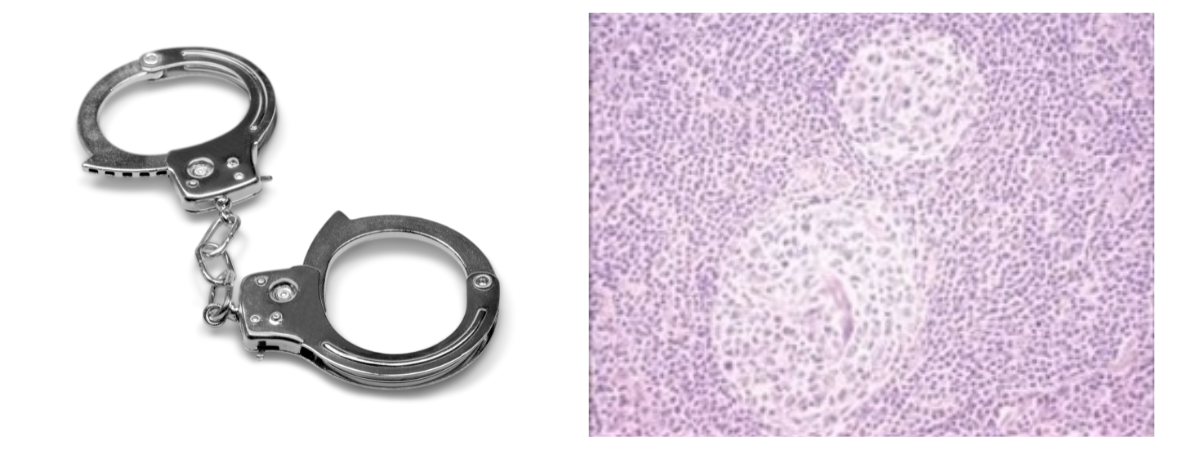
Un groupe de travail, en début d’année 2017, a redéfini les critères diagnostiques en proposant une nouvelle classification histologique pour les maladies de Castleman non associées au virus HHV-8 (David C. Fajgenbaum et al. Blood 2017;129:1646-1657). Ainsi, ils ont défini quatre types différents : la forme Hyaline-Vasculaire ou Hyper-Vasculaire (HV), la forme Plasmocytaire (PC) ou les formes Mixtes ou intermédiaires entre HV et PC. En plus de ces trois formes, il existe aussi la forme associée à HHV-8. Si vous souhaitez avoir plus de détails sur toutes les formes histologiques de MC, vous trouverez toutes les informations ici (casleman.fr).
Quelles sont les pathologies à prendre en compte dans le diagnostic différentiel de la maladie de Castleman ?
Concernant les différentes formes de la maladie de Castleman (MC), les principales pathologies qui peuvent faire état de diagnostics différentiels sont les suivantes :
Des pathologies malignes ou tumorales telles que :
- Le lymphome de Hodgkin (LNH) : encore appelé la maladie de Hodgkin, le LNH est lié à la prolifération incontrôlée de lymphocytes B anormaux appelés cellules de Reed-Sternberg. Il s’agit du principal diagnostic à écarter lors des premiers examens, en particulier chez les jeunes adultes. L’adénopathie (augmentation de la taille des ganglions) de Castleman et le LNH peuvent coexister chez un même patient, d’où l’importance d’examens poussés.
- Le lymphome non-hodgkinien : la différence entre le lymphome non-hodgkinien et le LNH est la présence de cellules de Reed-Sternberg, qui ne sont visibles que dans le cas d'un LNH. Il s’agit du second diagnostic à écarter pour les mêmes raisons que précédemment, en particulier dans le contexte d’une MC associée à HHV-8.
- Plasmocytome ganglionnaire : maladie rare, révélée par l’immunohistochimie (IHC) (méthode qui permet de détecter des marqueurs spécifiques dans les tissus) qui montre que les plasmocytes interfolliculaires (cellules dérivées de lymphocytes, sécrétant activement des anticorps) de la lésion de Castleman sont monotypiques, ou autrement dit uniformes.
- Le syndrome de POEMS (acronyme signifiant “polyneuropathie”, “organomégalie”, “endocrinopathie”, “hémopathie plasmocytaire” et “anomalies cutanées”) : dans sa forme classique, le syndrome de POEMS peut constituer un diagnostic différentiel. Certaines formes de MC peuvent en effet se compliquer de symptômes similaires au syndrome de POEMS (neuropathie, lésions cutanées …)
- Sarcome à cellules folliculaires dendritiques : Les sarcomes sont un groupe de nombreuses tumeurs cancéreuses qui se développent à partir de cellules issues du tissu de soutien de l’organisme. Il peut s’agir de tumeurs des "tissus mous" (tissu adipeux, muscles, vaisseaux, etc) ou des parties "dures" (os et cartilages) du corps.
Des pathologies inflammatoires ou auto-immunes telles que :
- Le lupus érythémateux systémique (LES) : c’est une maladie auto-immune (présence d’anticorps agressifs vis-à-vis de l'organisme) qui débute par des manifestations cutanées (lupus érythémateux) et évolue pour atteindre de nombreux organes (lupus érythémateux systémique). Il s’agit d’une maladie rare qui peut toucher la peau, les reins, les articulations, les poumons et le système nerveux. L’aspect des adénopathies dans le LES peut évoquer une MC. Toutefois, on ne retient pas le diagnostic de MC si celui de Lupus est établi.
- Le syndrome de Gougerot-Sjögren : maladie auto-immune rare touchant un peu moins d'un adulte sur 10 000, caractérisée par une infiltration de lymphocytes dans les glandes salivaires et lacrymales. Elle est responsable d'une sécheresse buccale et oculaire et de la production de différents auto-anticorps. Dans le diagnostic différentiel par rapport à une MC, la situation est superposable à celle du Lupus.
- La maladie de Still : encore appelée syndrome de Wissler-Fanconi, cette maladie rare cause un rhumatisme inflammatoire caractérisé principalement par des pics de fièvre au cours desquels surviennent des éruptions cutanées, accompagnées ou non de douleurs articulaires. Dans ce cas-ci, le diagnostic différentiel peut se révéler compliqué en l’absence de marqueur spécifique de la maladie de Still.
- L’arthrite chronique juvénile : inflammation des articulations se manifestant avant l’âge de 16 ans. Ici, dans le diagnostic différentiel par rapport à la MC, la situation est similaire à celle de la maladie de Still.
- La polyarthrite rhumatoïde (PR) : la plus fréquente des diverses formes de rhumatismes inflammatoires chroniques. Dans une PR active, les adénopathies en regard des arthrites peuvent avoir un aspect de Castleman.
- Des maladies associées aux IgG4 (immunoglobulines de type G4) : ici la question d’un diagnostic différentiel se pose du fait qu'un nombre conséquent de plasmocytes sécrétant des immunoglobuline (ou anticorps) de type IgG4 est parfois constaté dans la MC.
Des pathologies infectieuses telles que des primo-infections :
- À l’EBV (virus d’Epstein-Barr) : virus responsable de la mononucléose infectieuse (MNI). Les adénopathies associées à cette MNI peuvent avoir des similitudes avec la MC.
- Au CMV (cytomégalovirus) : virus souvent inoffensif, sauf pour les personnes immuno-déprimées et les femmes enceintes. Situation similaire à la MNI avec des adénopathies semblables à la MC.
- Au VIH (virus de l’immunodéficience humaine) : virus responsable du syndrome d'immunodéficience acquise (sida). Situation similaire à la MNI avec des adénopathies semblables à la MC.
- Au Toxoplasma gondii (responsable de la toxoplasmose) : situation similaire à la MNI avec des adénopathies semblables à la MC.
Des déficits immunitaires primitif, qui sont d’ordinaire présents à la naissance et sont des troubles génétiques généralement héréditaires :
- Déficit immunitaire commun variable (DICV) : trouble caractérisé par des taux d’immunoglobulines (anticorps) faibles et une prédisposition accrue aux infections. Les adénopathies du DICV, dans certaines formes, peuvent faire évoquer une MC. L’hypogammaglobulinémie (faible taux d’immunoglobuline dans le sang) permet de réorienter le diagnostic.
- Syndrome lymphoprolifératif auto-immun (SLAI, ou ALPS en anglais) : anomalie rare héréditaire caractérisée par une lymphoprolifération (multiplication anormale des globules blancs) non maligne et un risque accru tout au long de la vie de développer un lymphome Hodgkinien ou non-Hodgkinien. Là aussi, l’aspect des adénopathies peut évoquer une lésion de type Castleman. En cas de doute, l’analyse génétique confirmera le diagnostic.
- Déficit en ADA2 (adénosine désaminase 2) : maladie auto-inflammatoire liée à des mutations du gène ADA2. Contexte plutôt évocateur de vascularite systémique (inflammation des vaisseaux).
Le diagnostic définitif de la maladie de Castleman peut s’avérer compliqué, en particulier pour les formes plasmocytaires multicentriques idiopathiques. Celui-ci ne sera retenu qu’après avoir passé en revu et exclu un certain nombre de pathologies tumorales, infectieuses ou inflammatoires citées précédemment.
Le diagnostic de Maladie de Castleman impose un avis spécialisé, au mieux dans un centre de référence et à défaut en Hématologie ou Médecine Interne.
Si vous souhaitez avoir plus d’informations sur le diagnostic spécifique de la maladie de Castleman chez les enfants, rendez-vous sur notre article “Les enfants dans la maladie de Castleman”.
Pour aller plus loin :
N’hésitez pas à vous rendre sur le site du CDCN (Castleman Disease Collaborative Network) pour plus d'informations. Ce site est disponible en anglais uniquement.
Vous pouvez également rejoindre la communauté “Maladie de Castleman” sur Carenity pour partager votre expérience, trouver du soutien et échanger de l’information avec d’autres patients ou proches de patients.
Si faire entendre votre voix vous intéresse, faites-le nous savoir ! Partagez votre expérience et votre vécu (diagnostic, parcours…) dans la maladie de Castleman avec nos membres. Vous souhaitez témoigner ? Contactez nous à cette adresse : contact@carenity.com
Vous vous posez encore des questions sur le diagnostic et la prise en charge des patients Castleman en France ? Le Pr Jean-François Viallard, médecin interniste et chef du service de médecine interne de l’hôpital Haut-Lévêque du CHU de Bordeaux, répond à vos questions dans le podcast “Reconnaître la maladie de Castleman” réalisée par la chaîne RARE à L’écoute.
Sources :
Définitions d'hyperplasie, Dictionnaire médicale
Centre germinatif, Biologie cellulaire et moléculaire
Progeria : examen médical, Vulgaris médical
Lymphomes à cellules du manteau, Le portail des maladies rares et des médicaments orphelins
Définition : fibrose, Institut national du cancer
Le lymphome de Hodgkin, Gustave Roussy
Lymphome non hodgkinien : points clés, Institut national du cancer
Définition : sarcome, Institut national du cancer
Le lupus érythémateux systémique, Fédération des Maladies Dysimmunitaires
Le syndrome de Gougerot-Sjögren, Fédération des Maladies Dysimmunitaires
La maladie de Still de l’adulte, orpha.net
Déficit immunitaire commun variable, orpha.net
Commentaires
Vous aimerez aussi

Maladie de Castleman : “Nous devons sensibiliser la médecine et les médias à la maladie.”
21 déc. 2022 • 3 commentaires

Maladie de Castleman : "D’étudiant en médecine, je suis devenu patient."
18 sept. 2022 • 1 commentaire

 Facebook
Facebook Twitter
Twitter
